AutoEF — Schritt-für-Schritt Anleitung
Automatisierte Ejektionsfraktion (AutoEF) — Schritt-für-Schritt Anleitung für präzise Messung LV Volumen
Die automatisierte Ejektionsfraktion (AutoEF) ist ein semi-automatisches Messwerkzeug zur Bestimmung der globalen Ejektionsfraktion des linken Ventrikels. Diese Anleitung führt Sie systematisch durch die Vorbereitung, Bildakquisition, Durchführung der Analyse und Integration der Ergebnisse in den Untersuchungsablauf. Die Beschreibungen sind sachlich und präzise formuliert, Fachbegriffe werden in verständlicher Sprache erklärt.
Inhaltsverzeichnis
- Schritt 1: Vorbereitung und grundlegende Anforderungen
- Schritt 2: Systemstart und automatische Ansichtserkennung
- Schritt 3: Region of Interest (ROI) definieren
- Schritt 4: Prozessierung und Erkennung von Enddyastole/Endsystole
- Schritt 5: Nachbearbeitung der Frames und Konturen
- Schritt 6: Biplane‑Messung — zweite Ansicht hinzufügen
- Schritt 7: Prüfen, speichern und in den Befund überführen
- Schritt 8: FAQ
- Praktische Tipps zur Optimierung der Messqualität
- Verständliche Erklärungen wichtiger Fachbegriffe
- Interpretation der Ergebnisse
- Einschränkungen und klinische Grenzen
- Integration in den klinischen Workflow und Qualitätsmanagement
- Vergleich zu manuellen Messungen und anderen automatischen Methoden
- Fehlerbehebung: Häufige Probleme und Lösungen
- Abschluss: Entscheidende Punkte und Empfehlungen
- Kontaktinformationen für Gerätesupport und Schulungen
Schritt 1: Vorbereitung und grundlegende Anforderungen
Sie benötigen stabile Voraussetzungen, um zuverlässige AutoEF-Messungen zu erzielen. Achten Sie auf folgende Grundbedingungen:
- Stabile EKG-Kurve: Eine klare und stabile Elektrokardiogramm (EKG)‑Ableitung ist notwendig, da die Software End‑Systole und End‑Diastole über die Herzzyklusphasen erkennt.
- Apikale Ansichten: Mindestens eine apikale Vierkammer (APL4) und eine apikale Zweikammer (APL2) Ansicht in Form eines Loops (nur Speichern drücken, ohne vorher zu Freezen) sollten vorhanden sein. Für biplane EF werden beide Ansichten benötigt.
- Frame-Rate: Empfohlen ist eine Bildfrequenz > 40 Bilder pro Sekunde. Bei höheren Herzfrequenzen ist eine höhere Frame‑Rate notwendig, um die systolischen und diastolischen Zeitpunkte präzise zu erfassen.
- Kompletter LV-Myoardium: Das gesamte Myokard des linken Ventrikels muss innerhalb des Bildfelds sichtbar sein. Abschneiden der apikalen Region oder der Basen reduziert die Messgenauigkeit.
Diese Basis-Qualitätskriterien reduzieren Nachbearbeitung und verbessern die Konstanz gegenüber manuellen Messungen.
Schritt 2: Systemstart und automatische Ansichtserkennung
Öffnen Sie eine gespeicherte apikale Ansicht und wählen Sie die Mess‑Funktion. Navigieren Sie im Menü zur AutoEF‑Option und starten Sie das Tool.
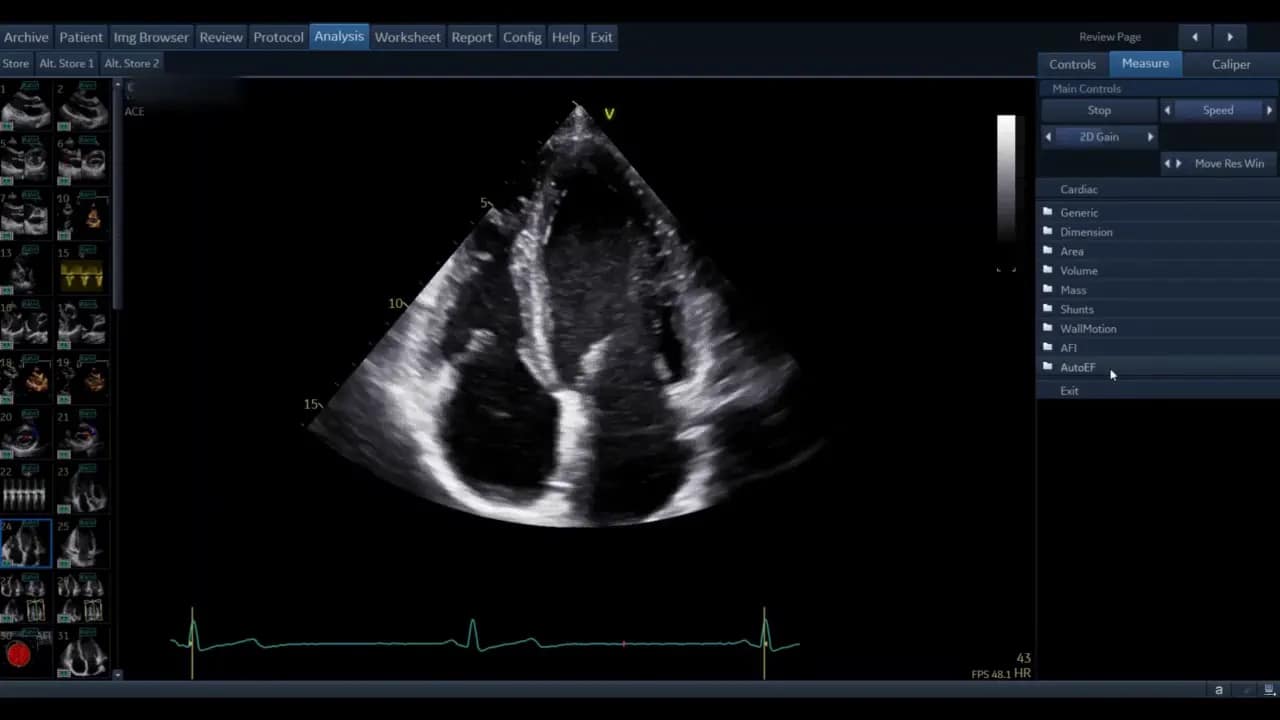
In aktuellen Versionen (abhängig von Modell und Softwarestand des Ultraschallgerätes) nutzt AutoEF eine View‑Recognition KI im Hintergrund. Diese findet automatisch die geeignetsten Vierkammer‑ und Zweikammer‑Bilder für die Analyse. Falls die automatische Erkennung fehlschlägt oder eine ältere Softwareversion verwendet wird, werden Sie aufgefordert, die Ansicht manuell zu wählen und zu kennzeichnen.
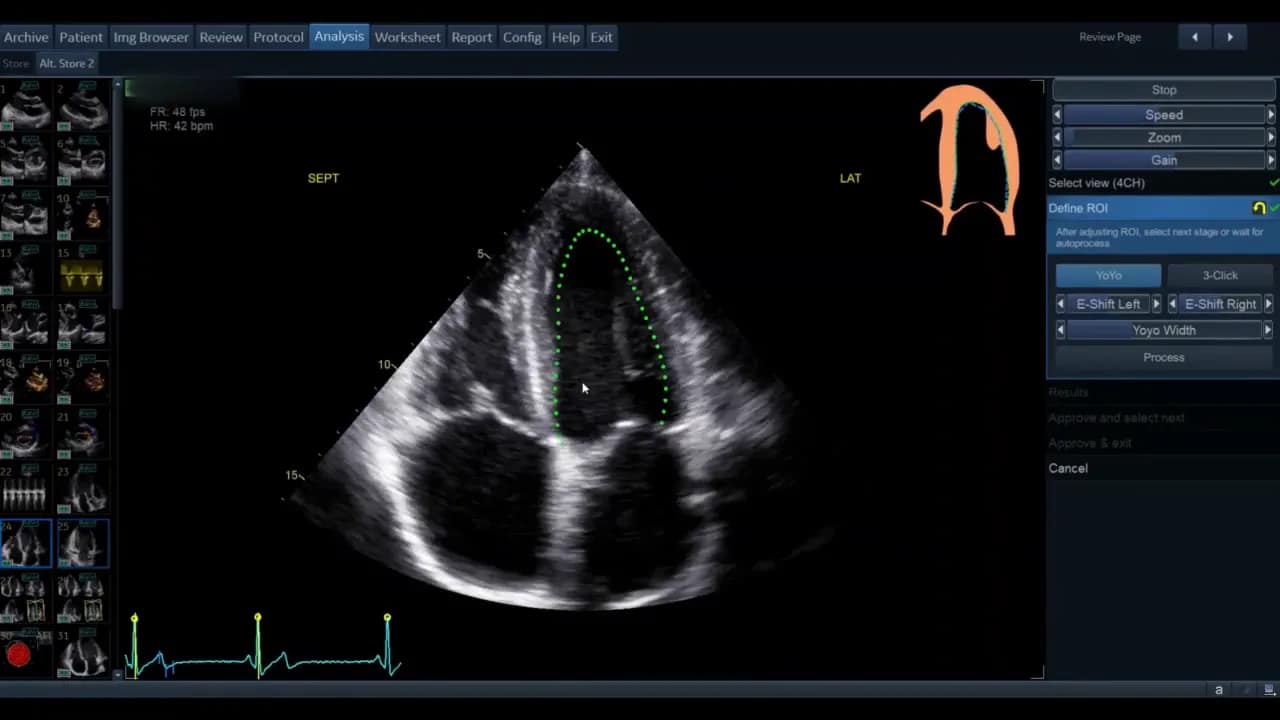
Wenn Sie manuell wählen müssen, markieren Sie zunächst die Vierkammer‑Ansicht, sofern diese als erstes analysiert werden soll. Die korrekte Kennzeichnung von septal, lateral und dem zugehörigen Piktogramm ist wichtig. Prüfen Sie, ob die Beschriftung mit der angezeigten Ansicht übereinstimmt, andernfalls zurück zur Auswahl und richtig taggen.
Schritt 3: Region of Interest (ROI) definieren
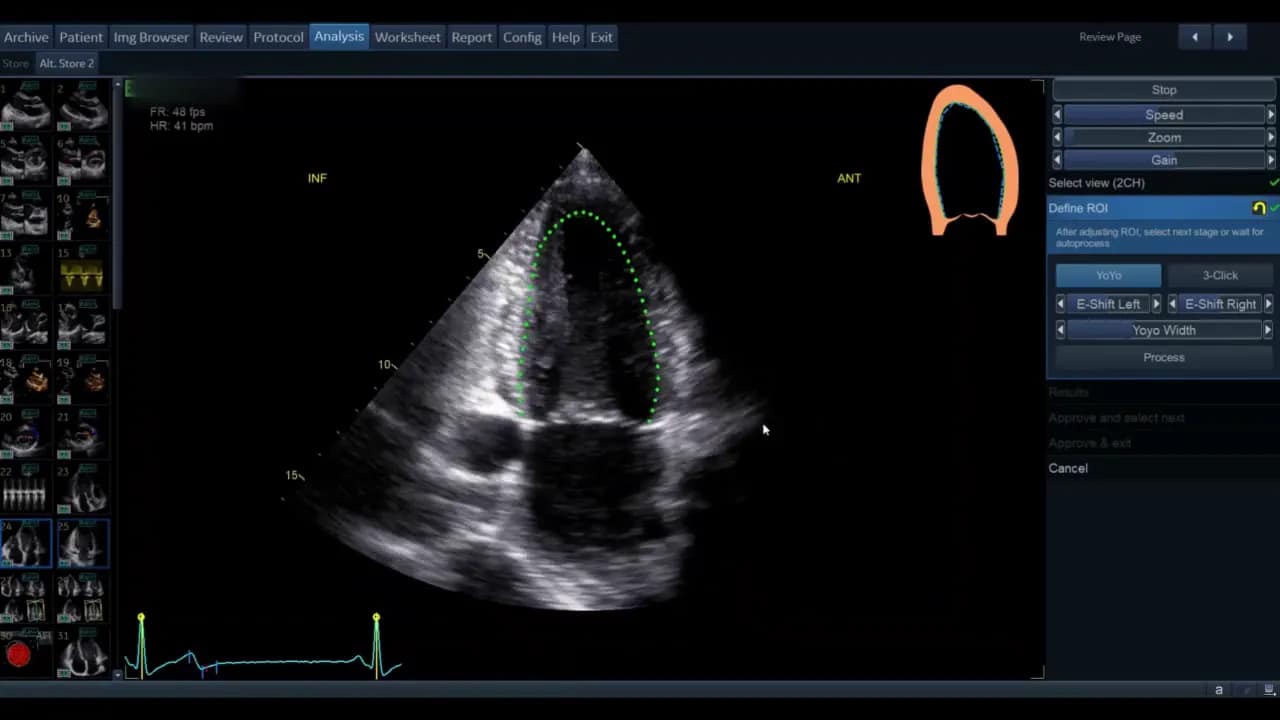
Sobald die Ansicht gewählt ist, gelangen Sie in die Phase der ROI‑Definition. Hier legt die Software die initiale Kontur für die automatische Wandsegmentverfolgung fest.
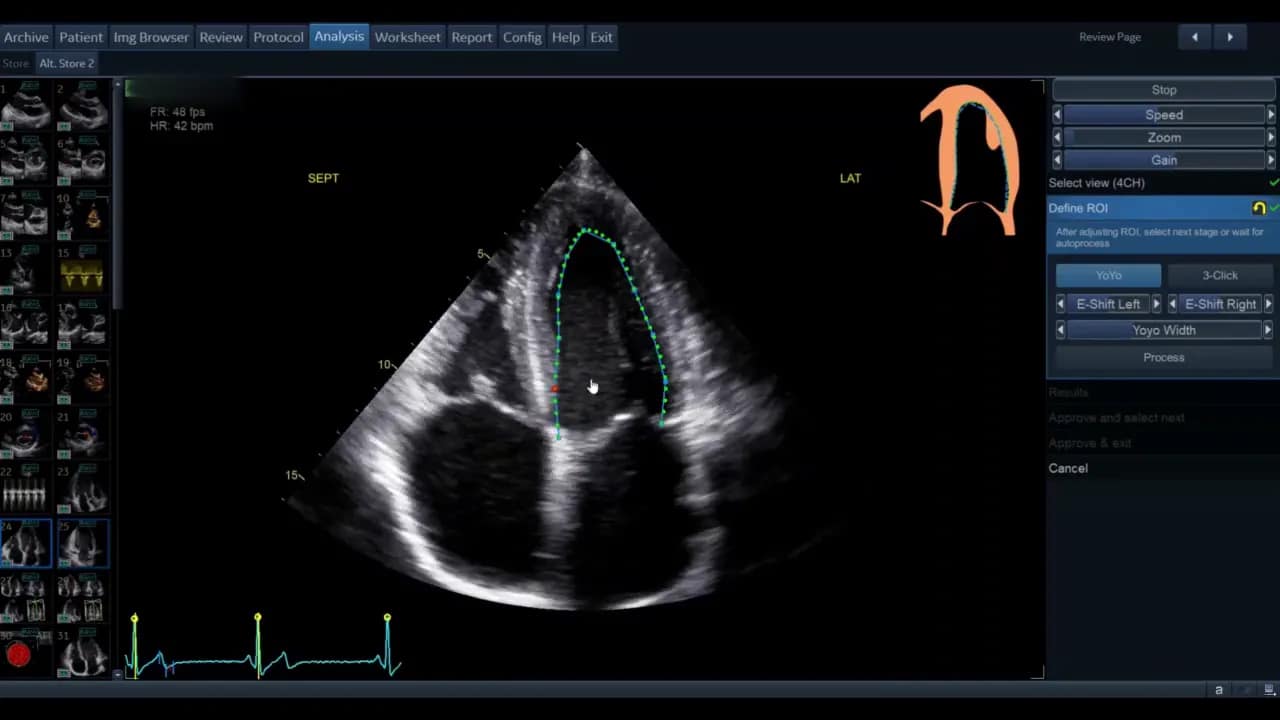
Die Standardkontur wird als grüne Linie (modellabhängig) angezeigt. Bewegen Sie den Cursor über diese Linie; rote Kreise erscheinen als Griffpunkte, die Sie anklicken, verschieben und loslassen können. Ziel ist eine möglichst genaue Platzierung entlang des inneren Myokardrandes ohne Papillarmuskeln und Trabekel zu ignorieren, soweit die Software dies zulässt.
- Wenn die vorgegebene Kontur passend ist, genügt das geringe Feintuning.
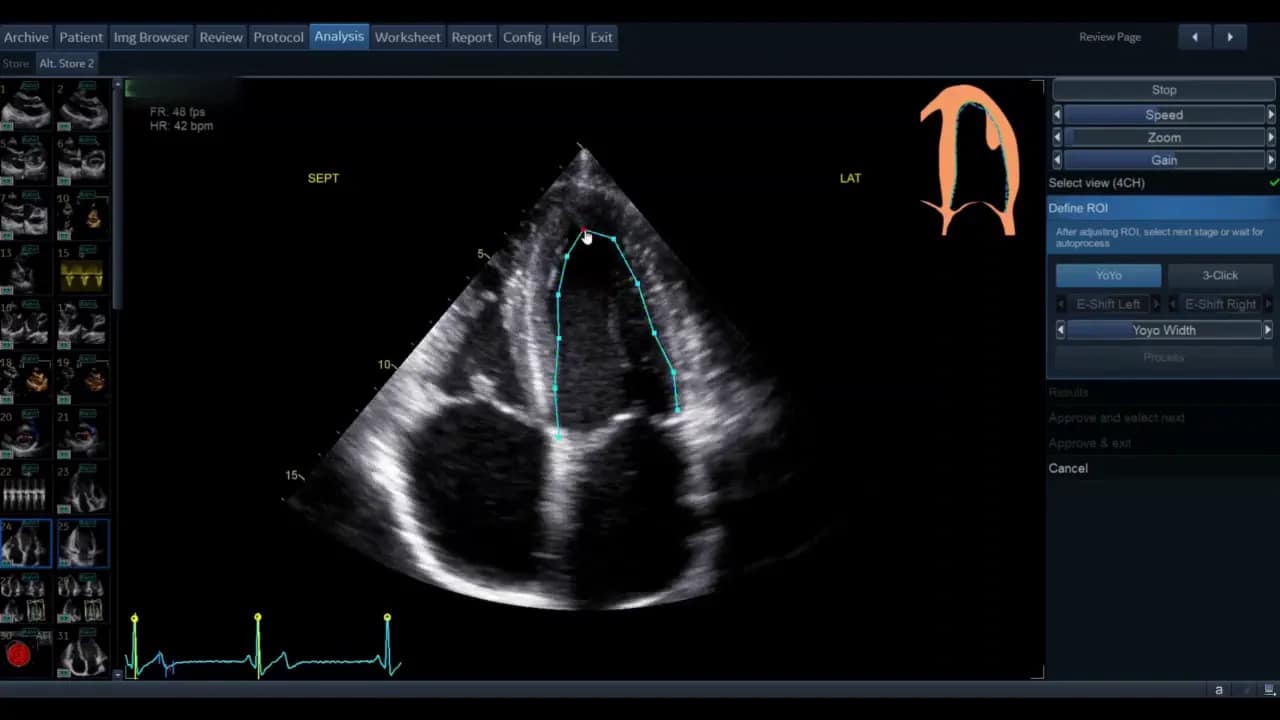
- Wenn die Kontur unbrauchbar erscheint, nutzen Sie die Drei‑Punkt‑Option. Dabei markieren Sie basal‑septal, basal‑lateral und den Apex manuell. Die Software interpoliert zwischen den Punkten.
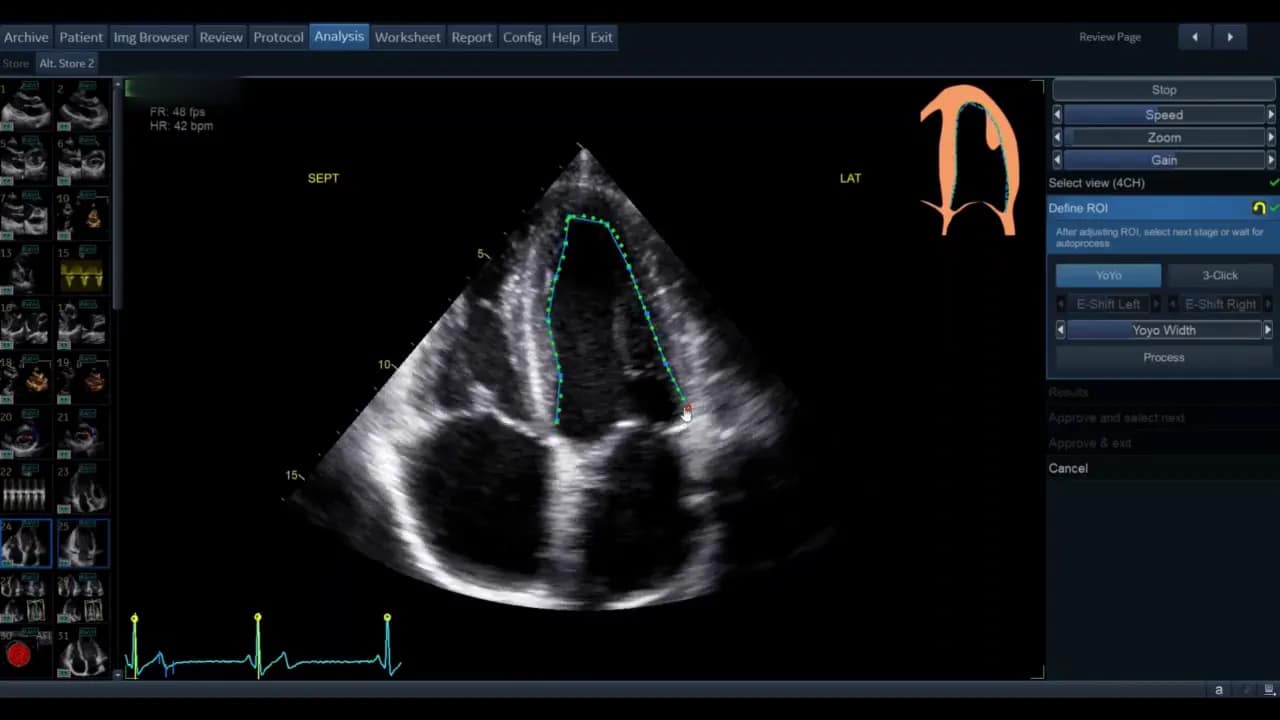
Nach der manuellen Markierung können Sie die so erzeugte grüne Kontur wiederum per Griffpunkte feinjustieren. Ziel ist, dass die Kontur den endokardialen Rand im gesamten Zyklus plausibel abdeckt.
Schritt 4: Prozessierung und Erkennung von Enddyastole/Endsystole
Klicken Sie auf Process, um die automatische Verfolgung starten zu lassen. Die Software identifiziert dann den Enddiastolen‑ und Endsystolen‑Frame.
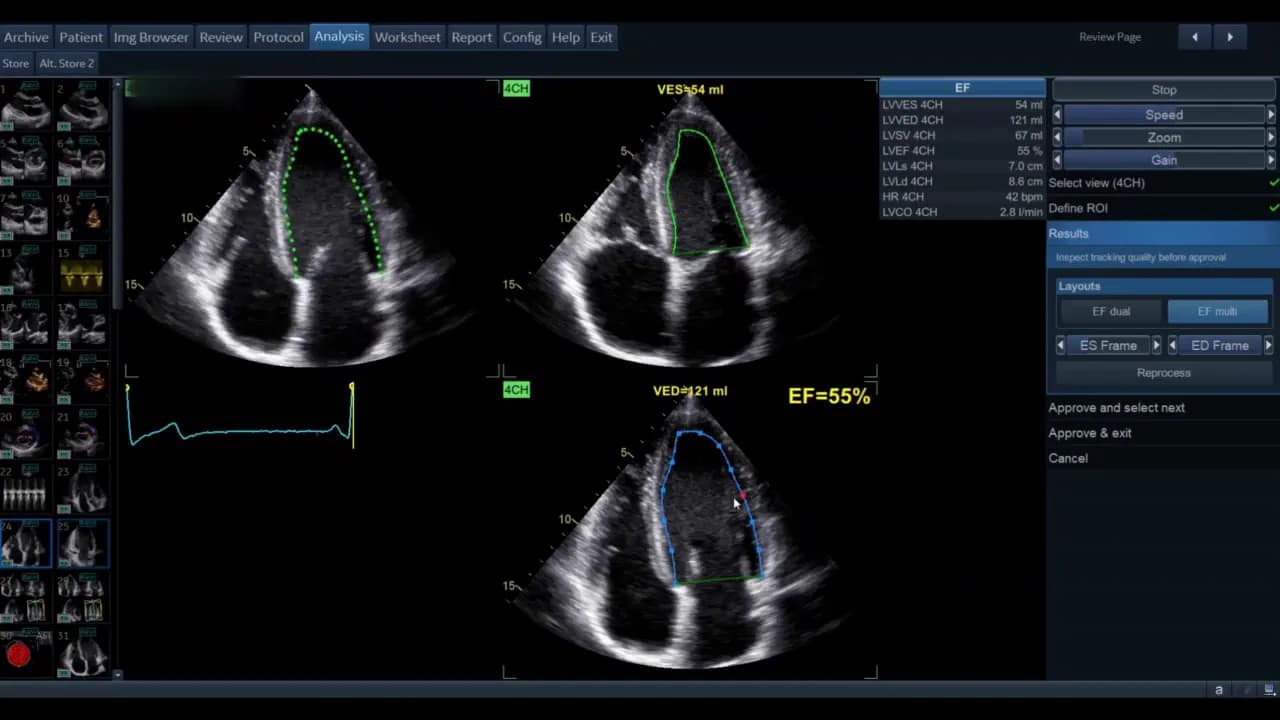
Enddiastole bezeichnet den Zeitpunkt maximaler Volumenfüllung des LV. Endsystole ist der Zeitpunkt minimalen LV‑Volumens. Diese Frames sind die Basis für die Volumenberechnung mittels Simpson‑Methode der Scheiben.
Die Ansicht kann als Einzelbild oder als EF‑Dual‑Display gezeigt werden. Im Dual‑Display sehen Sie gleichzeitig Systole und Diastole mit den berechneten Volumina und der Ejektionsfraktion als Prozentsatz.
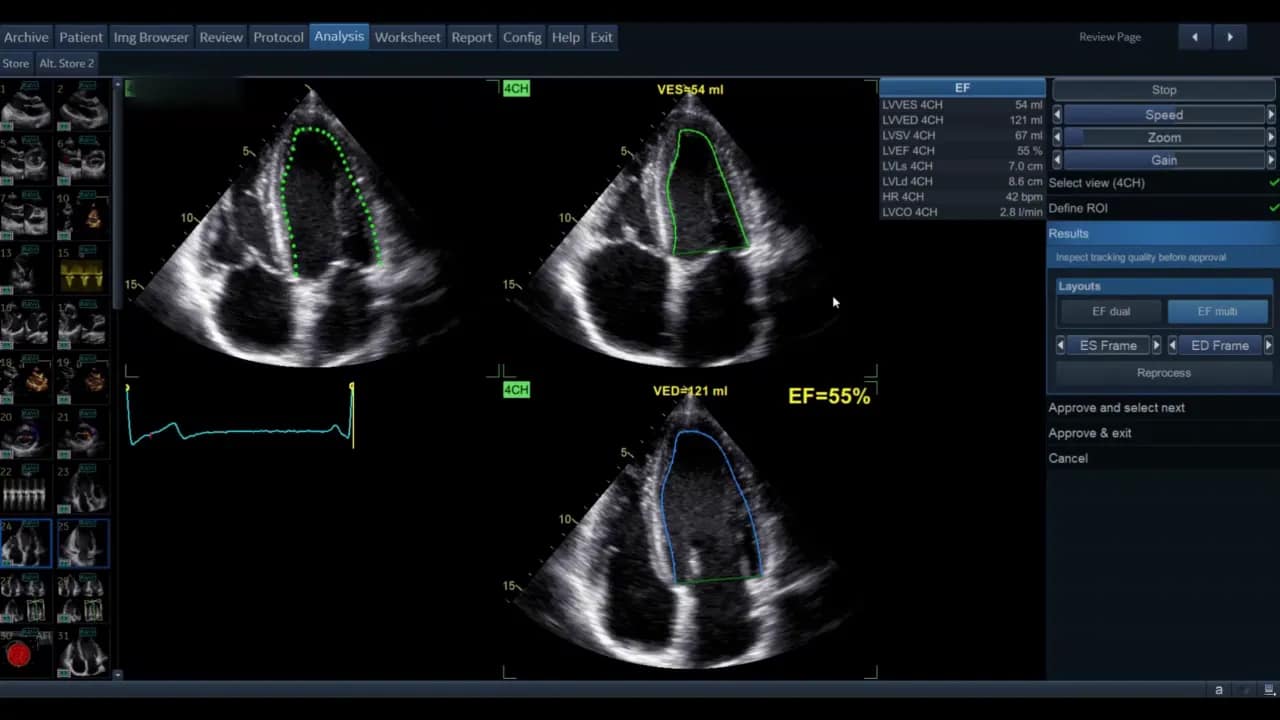
Speichern Sie die Ansicht jederzeit mit dem Store‑(Speichern-, P1-, modellabhängig) Button. So können Sie Zwischenergebnisse dokumentieren, bevor Sie weitere Anpassungen vornehmen.
Schritt 5: Nachbearbeitung der Frames und Konturen
Wenn die automatisch gewählten End‑Frames nicht korrekt sind, können Sie diese manuell auf der rechten Seite des Menüs ändern. Ebenso lassen sich Konturmarkierungen sowohl für systolische als auch diastolische Frames verschieben.
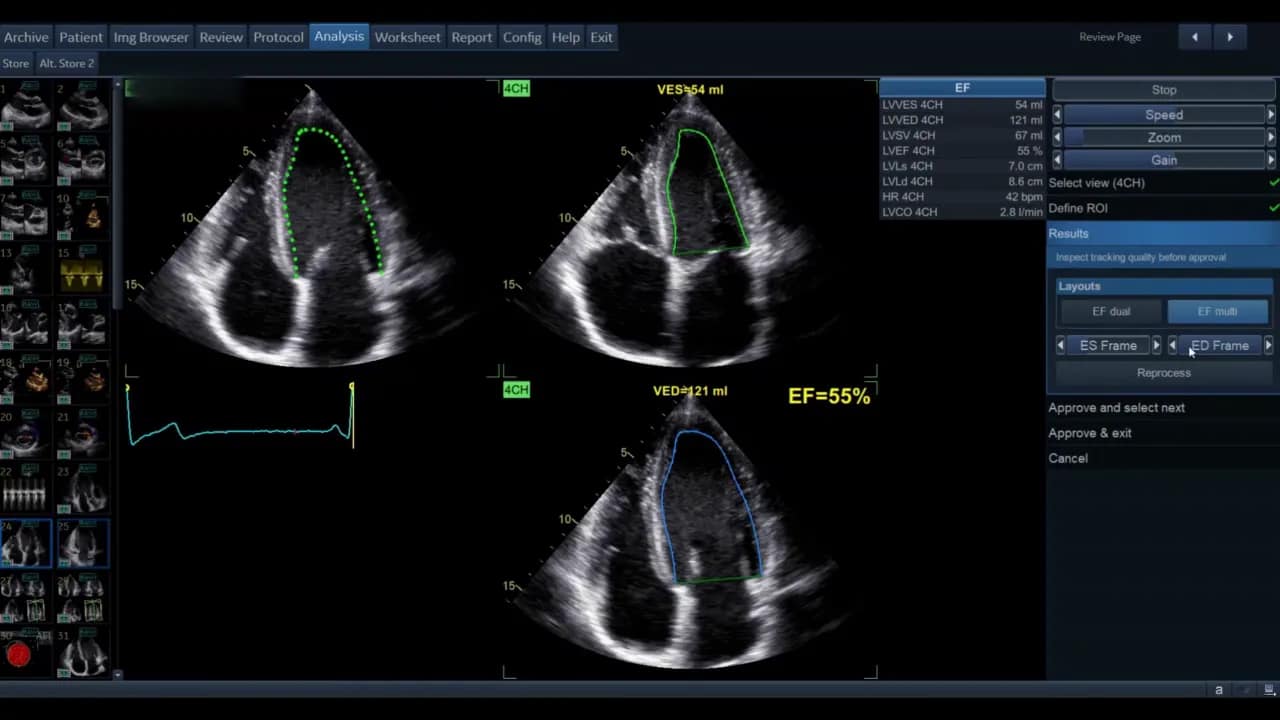
Wichtig: Jede manuelle Anpassung nach der initialen Prozessierung markiert das Ergebnis mit einem Sternchen. Dieses Sternchen signalisiert, dass Werte nachbearbeitet wurden. Wenn Sie Änderungen vor der endgültigen Auswertung sauber integrieren möchten, verwenden Sie die Reprocess Funktion, die eine erneute automatische Verfolgung nach Anpassung durchführt. So wird das Sternchen vermieden und die Konturoptimierung wird in den Algorithmus übernommen.
Schritt 6: Biplane‑Messung — zweite Ansicht hinzufügen
Für die standardisierte Ejektionsfraktionsbestimmung wird häufig die modifizierte biplane Simpson‑Methode verwendet. Dazu müssen die Werte aus APL4 und APL2 kombiniert werden. Nach Freigabe der Vierkammer‑Ansicht wählen Sie Approve und Next. Die View‑Recognition sollte automatisch die passende Zweikammer‑Ansicht anzeigen.
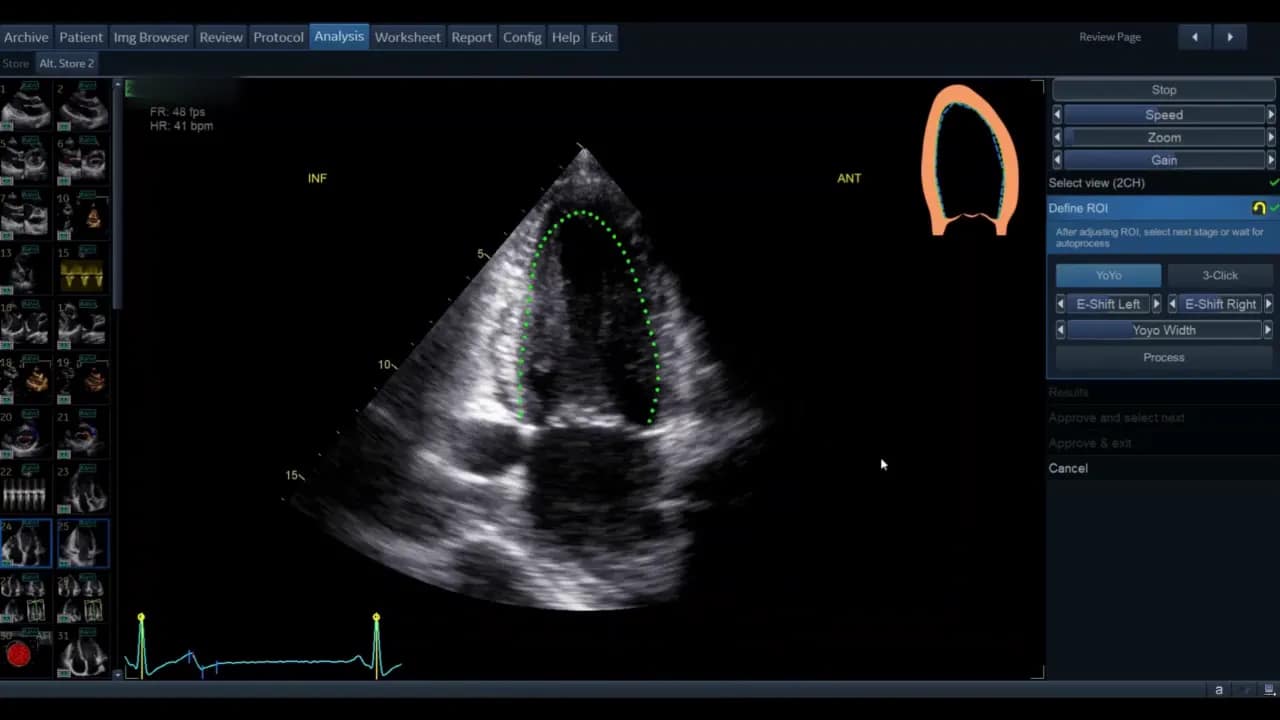
Wenn AutoEF die Ansicht nicht automatisch korrekt identifiziert, wählen Sie manuell die passende APL2‑Aufnahme aus und markieren sie entsprechend. Wiederholen Sie die ROI‑Definition, Prozessierung und gegebenenfalls Nachbearbeitung analog zur ersten Ansicht.
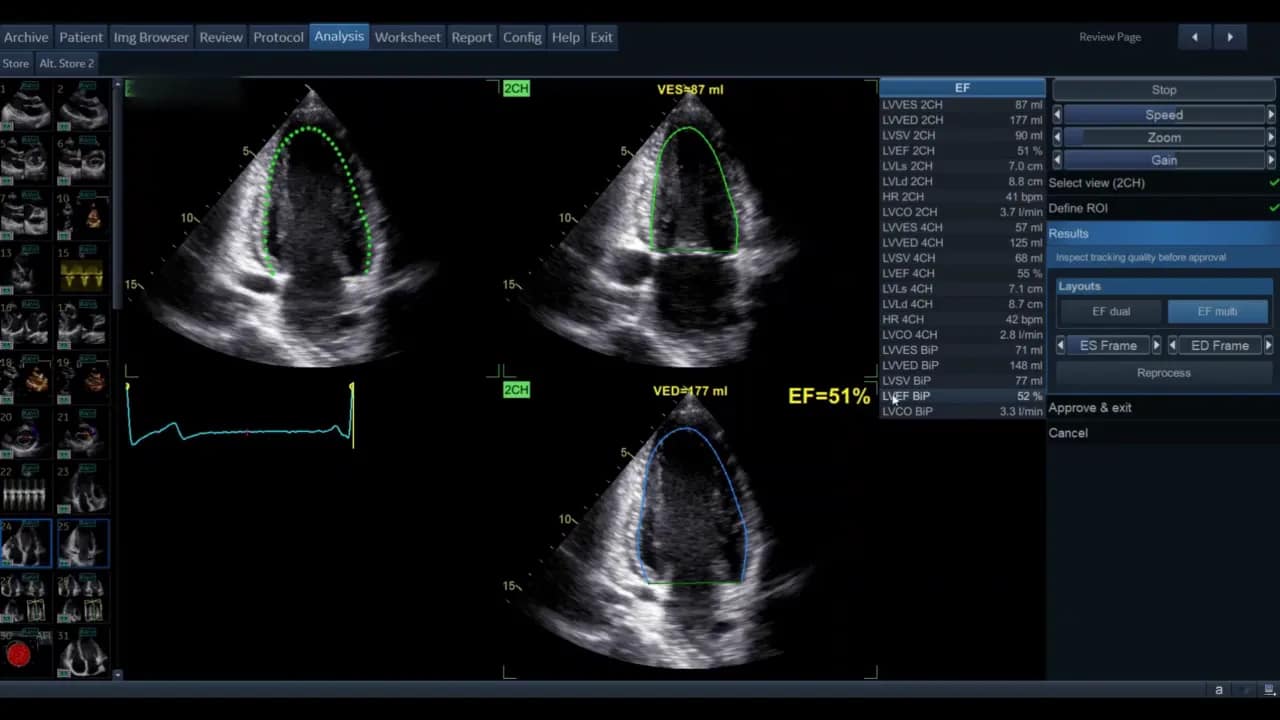
Die Software zeigt nach erfolgreichem Durchlauf die systolischen und diastolischen Volumina beider Ansichten sowie die berechnete biplane Ejektionsfraktion. Diese Werte erscheinen in der Ergebnisliste; die biplane EF wird in der Regel als kombinierter Wert ausgewiesen.
Schritt 7: Prüfen, speichern und in den Befund überführen
Vor Abschluss sollten Sie folgende Punkte nochmals prüfen:
- Stimmen die End‑Frames für Systole und Diastole mit den visuellen Maxima und Minima überein?
- Deckt die Kontur das endokardiale Myokard präzise ab?
- Sind Papillarmuskeln nicht fälschlich als Blutpool interpretiert worden?
Wenn Sie zufrieden sind, wählen Sie Approve and Exit. Die Messwerte werden in das Arbeitsblatt bzw. in die Messliste übernommen. Wollen Sie die Ergebnisse verwerfen, wählen Sie Cancel.
Schritt 8: FAQ
Welche Bildqualität ist minimal erforderlich, damit AutoEF zuverlässig arbeitet?
Mindestens zwei apikale Ansichten (APL4 und APL2) mit einer Frame‑Rate über 40 fps und einem vollständigen Sichtfeld des linken Ventrikels. Eine stabile EKG‑Ableitung ist ebenfalls erforderlich, damit End‑Systole und End‑Diastole korrekt identifiziert werden.
Wann sollte ich die Drei‑Punkt‑Option zur ROI‑Definition verwenden?
Wenn die automatische Kontur stark abweicht oder z. B. der Apex nicht korrekt erfasst wird. Mit der Drei‑Punkt‑Methode setzen Sie basal‑septal, basal‑lateral und Apex manuell und erhalten eine bessere Ausgangskontur.
Was tun, wenn Teile der Kontur rot statt grün dargestellt werden?
Rot zeigt an, dass die Tracking‑Qualität lokal unzureichend ist. Machen Sie eine kleine manuelle Korrektur der Kontur oder reprocessen Sie die Ansicht, bis die Kontur in den betroffenen Segmenten grün wird.
Wie wird die Ejektionsfraktion berechnet?
Für jede Ansicht verwendet das System die Simpson‑Methode der Scheiben: Das Volumen wird aus einer Serie von Scheiben entlang der longitudialen Achse errechnet. Für die globale biplane EF kombiniert die Software die Volumina aus der APL4 und APL2 gemäß der modifizierten biplanen Simpson‑Methode.
Sind AutoEF‑Werte genauso zuverlässig wie manuelle Messungen?
AutoEF reduziert Anwender‑Variabilität und spart Zeit. Ergebnisse sind oft vergleichbar oder besser reproduzierbar als manuelle Messungen, vorausgesetzt die Aufnahmequalität ist ausreichend. Dennoch bleibt klinische Plausibilitätsprüfung durch den Untersucher notwendig.
Welche Fehlerquellen sind typisch?
Unvollständige Apikalansicht, schlechte EKG‑Signale, Artefakte, zu niedrige Frame‑Rate, bewegungsbedingte Verzerrungen oder unzureichende Konturdefinition durch starke Trabekelbildung. Solche Faktoren können zu fehlerhaften Volumen‑ oder EF‑Werten führen.
Wie dokumentiere ich, dass eine AutoEF‑Messung durchgeführt wurde?
Speichern Sie die annotierten Bilder und fügen Sie die Messergebnisse dem Befundblatt hinzu. Viele Systeme kennzeichnen automatisch, ob eine Messung reprocessed oder manuell angepasst wurde.
Praktische Tipps zur Optimierung der Messqualität
Die beste Automatik nützt wenig, wenn die Eingabedaten suboptimal sind. Nachfolgend bewährte Maßnahmen für konsistente Ergebnisse:
- Patientenposition: Optimieren Sie die Lagerung, um apikale Fenster maximal zugänglich zu machen. Rollen Sie den Patienten leicht zu Ihnen hin, um die apikale Sicht zu verbessern.
- Schallkopforientierung: Achten Sie auf den optimalen Schallkeil; kleine Winkeländerungen verbessern oft Apex‑Darstellung.
- Bildgröße und Tiefeneinstellung: Verkleinern Sie die Tiefe, so dass der LV gut ausgefüllt wird, ohne dass benachbarte Regionen abgeschnitten sind.
- Transducer‑Fokus: Setzen Sie den Fokus auf die Region des LV, um Konturen schärfer zu erhalten.
- Vermeiden Sie zu starke Bildverarbeitung: Aggressive Glättungsfilter können endokardiale Strukturen verwischen und Tracking stören.
Verständliche Erklärungen wichtiger Fachbegriffe
Ejektionsfraktion (EF): Anteil des Blutvolumens, das der linke Ventrikel bei der Systole auswirft, ausgedrückt als Prozent des enddiastolischen Volumens. Clinically relevant: Werte unter 40% deuten üblicherweise auf eine systolische Dysfunktion hin.
Simpson‑Methode: Volumenberechnung durch Aufteilung des Ventrikels in mehrere diskrete Scheiben (Discs) entlang der Longitudinalachse. Für jede Scheibe werden Durchmesser und Volumen berechnet und summiert, um das Gesamtvolumen zu erhalten.
Biplane EF: Kombinierter EF‑Wert, der aus zwei orthogonalen apikal‑projektionen (APL4 und APL2) ermittelt wird. Dieser Ansatz reduziert Fehler, die aus Projektionseffekten einer einzelnen Ansicht entstehen können.
Interpretation der Ergebnisse
Die AutoEF liefert Volumina für EDV (end‑diastolic volume) und ESV (end‑systolic volume) sowie die EF. Interpretieren Sie die Werte im klinischen Zusammenhang:
- Leicht reduzierte EF (40–49%) kann auf beginnende systolische Dysfunktion hinweisen.
- Moderat bis stark reduziert (< 40%) erfordert weiterführende Diagnostik und Therapieüberlegungen.
- Grenzwerte variieren je nach Leitlinie und Patientenpopulation; vergleichen Sie gegebenenfalls mit Vorbefunden.
Bei Plausibilitätsfragen überprüfen Sie Bildqualität, Nachbearbeitungsmarker und ob eine manuelle Korrektur notwendig ist.
Einschränkungen und klinische Grenzen
AutoEF ist ein leistungsfähiges Tool, ersetzt aber nicht die klinische Beurteilung. Typische Einschränkungen:
- Unvollständige Sicht des Apex führt zu systematisch niedrigeren Volumina.
- Starke Wandbewegungsstörungen oder Aneurysmata können die automatische Segmentierung verwirren.
- Starkes Vorhandensein von Trabekeln und Papillarmuskeln kann die Trennung von Blutpool und Endokard erschweren.
In diesen Fällen ist eine manuelle oder halbautomatische Nachbearbeitung oft erforderlich. Dokumentieren Sie Anpassungen transparent.
Integration in den klinischen Workflow und Qualitätsmanagement
AutoEF kann Arbeitsabläufe beschleunigen und Messvarianz reduzieren. Zur erfolgreichen Integration empfiehlt sich:
- Schulung des Bedienpersonals in Bildakquisition und Nachbearbeitung.
- Standardisierte Protokolle für apikale Aufnahmen, Frame‑Rate und Speicherformate.
- Regelmäßige interne Qualitätskontrollen durch Vergleich von AutoEF mit manuellen Messungen.
- Protokoll zur Dokumentation von Nachbearbeitungen und Sternchen‑Markierungen.
Langfristig verbessert dies die Datenkonsistenz, erleichtert Vergleichsanalysen und steigert die Nutzerakzeptanz.
Vergleich zu manuellen Messungen und anderen automatischen Methoden
Automatische Algorithmen sind schneller und oft reproduzierbarer als manuelle Free‑hand‑Messungen. Allerdings liefern sie nur dann optimale Ergebnisse, wenn die Rohdaten hochwertig sind. Manualer Aufwand bleibt in bestimmten Fällen unverzichtbar:
- Extensive Wandnarben oder schlechte Akustik erfordern Expertenkorrektur.
- Zwei‑D‑Techniken haben Limitationen gegenüber 3D‑Volumenmessungen; aber 3D ist nicht immer praktisch oder verfügbar.
Die Wahl zwischen AutoEF, manueller Simpson‑Messung und 3D hängt von klinischer Fragestellung, Bildqualität und verfügbarem Equipment ab.
Fehlerbehebung: Häufige Probleme und Lösungen
Typische Probleme und pragmatische Lösungen:
- Problem: Kontur ist ungenau, rote Segmente angezeigt. Lösung: Kleine manuelle Korrekturen oder erneutes Reprocess; prüfen Sie Bildfrequenz und Bildfeld.
- Problem: Apex abgeschnitten. Lösung: Neuaufnahme mit kleinerer Tiefe bzw. besserer Schallkopfposition.
- Problem: Unklare End‑Frames. Lösung: EKG‑Ableitung überprüfen, höhere Frame‑Rate verwenden oder Frames manuell setzen.
- Problem: Automatische Ansichtserkennung wählt falsche Bilder. Lösung: Manuelle Auswahl und Kennzeichnung der korrekten Ansichten.
Abschluss: Entscheidende Punkte und Empfehlungen
AutoEF bietet eine effiziente Möglichkeit, LV‑Volumina und EF zu bestimmen. Die wichtigsten Erfolgsfaktoren sind:
- Hohe Bildqualität mit ausreichender Frame‑Rate.
- Sorgfältige ROI‑Definition und Plausibilitätsprüfung durch den Untersucher.
- Dokumentation manueller Anpassungen und regelmäßige Qualitätssicherung.
Wenn Sie diese Punkte beachten, reduziert AutoEF Messfehler, spart Zeit und liefert reproducible Ergebnisse, die im klinischen Alltag zuverlässig verwendbar sind.
Kontaktinformationen für Gerätesupport und Schulungen
Für produkt‑ oder softwarespezifische Fragen, Schulungen oder Integration in Ihr PACS/Worflowsystem kontaktieren Sie Ihren technischen Ansprechpartner bei ROWAMED. Regelmäßige Trainings stärken die Konsistenz in der Bildakquisition und reduzieren Nachbearbeitungsbedarf.
